在蛋白质分子中的“蝴蝶效应” - 改变3个原子会导致大效果
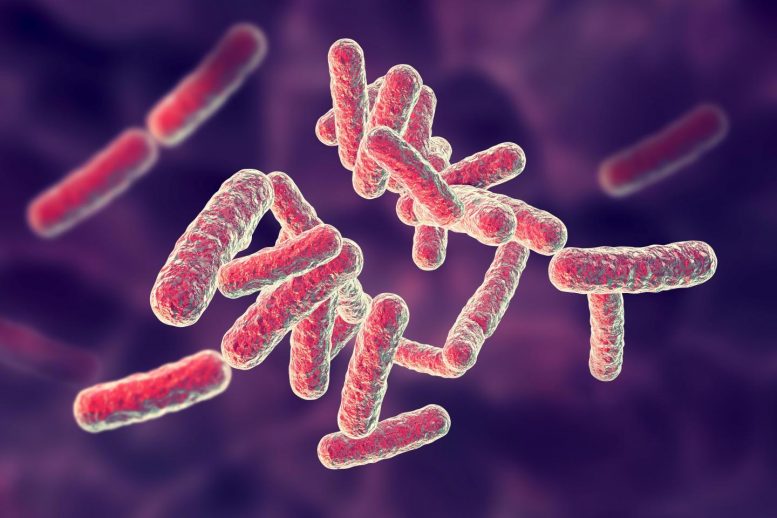
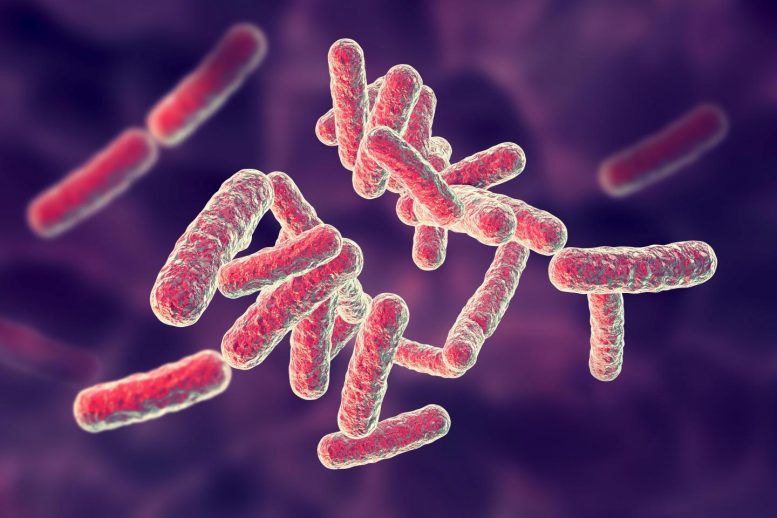
病原细菌,志贺氏菌是每年腹泻相关死亡的主要原因。
“蝴蝶的翅膀在巴西翅膀的翅膀掀起了德克萨斯州的龙卷风吗?” - 在美国科学促进协会第139次会议上,爱德华洛伦茨
最近发现科学家发现了蛋白质分子中3个原子中的微量变化的机制可以影响细胞中的免疫信号。这种“蝴蝶效应”由细菌,志贺氏菌,志贺氏菌,在它感染的宿主细胞内存活。
Ranabir Das'团队在全国生物科学中心(NCBS),班加罗尔发现,由细菌酶引起的蛋白质UBC13的微小变化产生了级联的小原子改变,直到它们防止UBC13束缚对伴侣蛋白,TRAF6。在没有UBC13-Traf6复合物的情况下,宿主细胞不能开始对细菌的免疫应答发出信号。本研究探讨了一个微妙的改变的机制 - 涉及只有3个原子的丧失 - 并调查它如何具有深远的后果。
根据数学的混沌理论,一分钟的变化,如“蝴蝶翼”的“襟翼”可能会导致其他地方的巨大变化。这似乎在较小的尺度上保持真实 - 例如,在一个小区内。来自国家生物科学中心(NCBS),班加罗尔的科学家现在已经发现了蛋白质分子中的小型原子变化使细菌能够关闭其宿主的免疫信号系统。
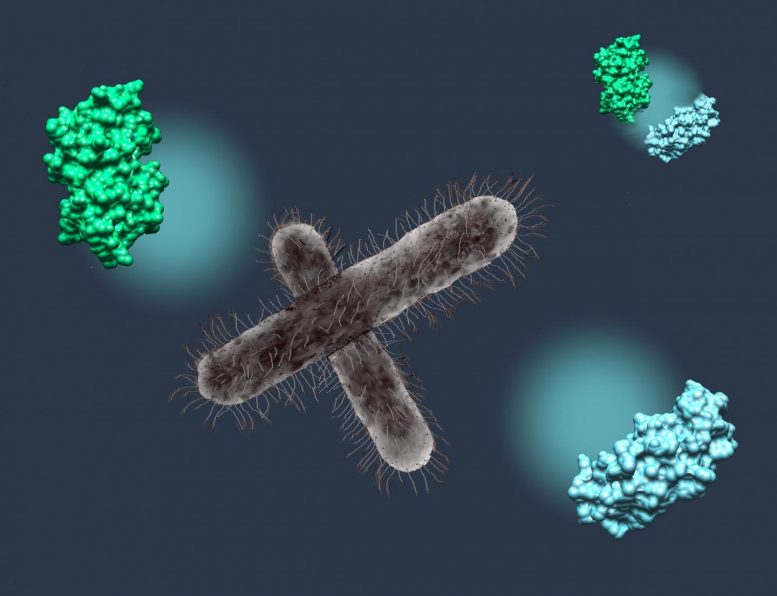
病原细菌志贺氏菌(中枢)可防止人蛋白UBC13(绿色)和Traf6(蓝色)的结合来破坏人宿主细胞的免疫应答。
Shigella Flexneri是一种偷偷摸摸和高度感染的细菌。导致人类腹泻的生物,首先附着在宿主肠道的细胞上。然后使用针状设备,S.Flexeri开始泵送其秘密武器 - 一种在宿主细胞蛋白UBC13中改变单个氨基酸的酶(遍兴蛋白缀合酶E2 13)。这种变化呈UBC13无法与伴侣蛋白质Traf6(肿瘤坏死因子相关因子6)结合,并且有效地阻断宿主细胞以用于炎症反应的信号传导。随后,志贺氏渗入宿主细胞以乘以。
之前,讨论了如何微妙的效应 - 在含有大约3000个原子的蛋白质分子中的3个原子的变化很少 - 可以关闭宿主的免疫应答。
然而,Ranabir Das'团队在NCBS的新研究表明,当从宿主蛋白UBC13中的单个氨基酸中从单个氨基酸中除去胺基(由一个氮和两个氢原子形成)时,一系列相对小的原子变化堆积起来阻止免疫应答途径的关键步骤。从塔塔基本研究所和印度生物技术部获得资金支持的工作已在Elife期刊上作为一文发表。
“我们使用了结构研究,计算建模和酶实验的组合,发现UBC13的原子变化不会改变其结构。相反,这些变化完全破坏了其绑定其伴侣蛋白的能力TRAF6,“Priyesh Mohanty说,他们是DAS'团队的一部分,以及描述这些结果的论文中的第一个作者。
当从宿主蛋白UBC13中的单个氨基酸中除去胺基(由一个氮和两个氢原子形成),一系列相对小的原子变化堆积起来,以阻止免疫应答途径的关键步骤。
UBC13中的第14个氨基酸,一种精氨酸残基(精氨酸14)是关键在于在形成'盐桥 - 与Traf6之间的粘合剂之间的粘合剂。该两种蛋白质的表面之间的该盐桥是稳定和维持UBC13-Traf6复合物,其又在免疫响应信号传导中起着枢转作用。当细菌酶命名为OSPL,达到谷氨酰胺残基(谷氨酰胺100)时,通过带负电荷的羟基代替中性胺基。现在,该集团从UBC13-Traf6间盐桥中偷走了精氨酸14,以形成一个分子内盐桥。反过来,这损害了UBC13和TRAF6之间的瞬态相互作用,这是形成最终复合物所必需的。最后,UBC13表面上的新负电荷在UBC13和TRAF6蛋白之间产生瞬态排斥力。
盐桥和表面有吸引力的力集体创造了足够强大的力,以稳定(或保持)UBC13-Traf6复合物。随着这些力的丧失,复合物分开,而没有复合物,对细菌的免疫信号被阻断。
“这项调查确实有助于我们了解杀虫氨基酸在蛋白质和蛋白质在细胞内的关联中的作用,”说Mohanty和Das。“据我们所知,我们的研究是第一个提供谷氨酰胺脱染靶蛋白的机制的机制阻碍了宿主细胞内的功能。有趣的是,这种机制使细菌能够衰减炎症反应并促进其在人类宿主中存活的能力,“他们补充道。
目前,由于每年腹泻导致令人痛苦的次数差不多有2%的死亡,其中三分之一发生在婴儿。这些细菌的几种多药抗性也出现,但是没有疫苗或药物来防止或限制志贺氏爆发的蔓延。
“因此,研究志贺卡用于衰减人体宿主中的炎症反应的机制非常重要。这些研究可能有助于研究人员识别可以控制人类疾病的新药,“穆罕默德和DAS说。
参考:“脱次破坏了本土和瞬态接触,削弱了UBC13和戒指 - 手指E3连接之间的互动”,由Priyesh Mohanty,Rashmi Altata,Batul Ismail Habibullah,Arun Geetha Surendran和Ranabir Das,2019年10月22日,Elife.Doi:
10.7554 / Elife.49223
-
研究人员演化了消耗CO2的细菌的能量
2022-03-12 -
有价值的2D材料,脱臼,在银中自由生长到原子的“皮肤”中
2022-03-09 -
在加热时缩小晶体后面的迷人秘密
2022-03-09 -
母乳中发现的化合物可对抗有害细菌-可以添加到配方奶或牛奶中
2022-03-08 -
生物膜在空间和设备和宇航员的风险
2022-03-08 -
致命病原体的快速进化:霍乱细菌一口气可盗取多达150个基因
2022-03-07 -
细菌生活方式改变抗生素抗性的演变
2022-03-07 -
新药&“绿色”杀虫剂可以有效合成银杏化合物
2022-03-07 -
物理学家用量子力学双子悖论对爱因斯坦进行了测试
2022-03-07 -
原子能级成像可以使金属具有前所未有的特性
2022-03-06 -
水三明治的量子稳定化 - 古典物理学法则分解
2022-03-06 -
高效的量子力学界面导致光与物质之间的强相互作用
2022-03-06 -
鲨鱼皮肤微生物组可保护伤口免受感染
2022-03-06 -
Picoscience和可以模仿神经元的新材料,用磁铁计算
2022-03-06 -
达尔文矛盾:最友好细菌的生存
2022-03-06