UCLA研究人员揭示了修复MS损坏的神经的潜在途径
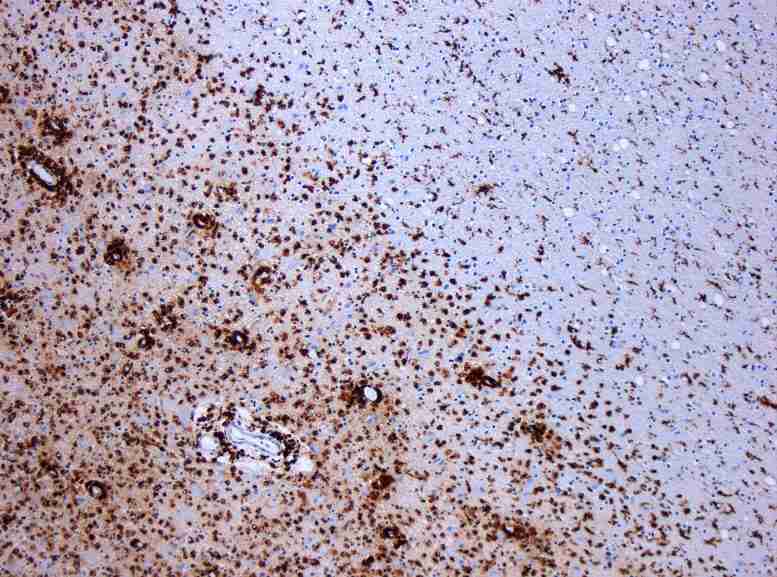
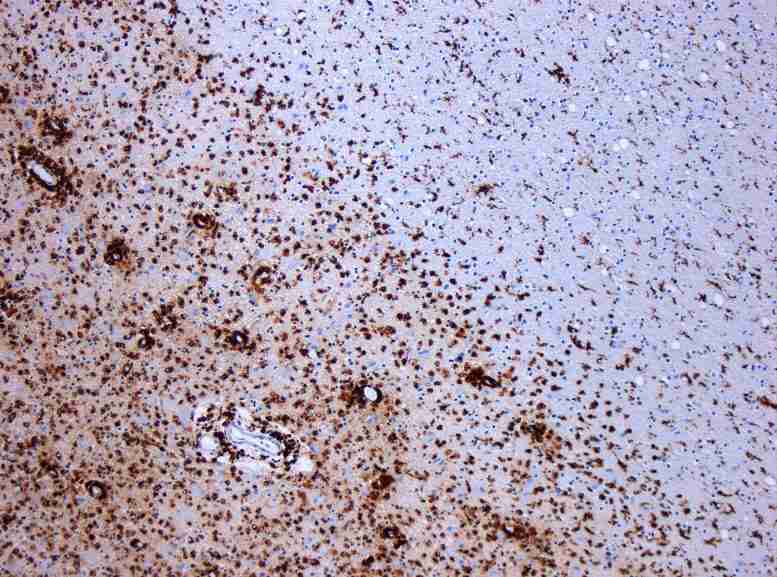
MS的脱髓鞘。CD68彩色组织显示出病变区域的几种巨噬细胞。维基百科
发现
特定细胞和特定区域的基因表达可以提供比传统神经疾病治疗更精确的神经保护方法。对于多发性硬化,具体而言,增加脊髓星形胶质细胞中的胆固醇合成基因表达可以是修复影响行走的神经的途径。
背景
多发性硬化是一种自身免疫性,神经变性疾病,其特征在于影响行走,视觉和认知的不同残疾,称之为一些。MS患者彼此有所不同,关于哪些残疾最多影响它们。炎症从神经电池延伸,称为轴突和神经末端的连接,称为突触,丢失,在一起,在这种情况下,将信号传导和最终引起永久性残疾,称为突触,并根据这发生这种情况,造成突出物。UCLA研究人员提出,每种残疾背后的分子机制可能不同,并且对于每种残疾量身定制的神经保护处理可能比旨在减少不同残疾的复合材料的非特异性治疗更有效。该团队专注于星形胶质细胞,一种在MS中激活的脑细胞,并在疾病中发挥几个重要作用,在不同地区的星形胶质细胞中检查基因表达。
方法
使用MS的小鼠模型,研究小组评估了脑和脊髓的各个区域的星形胶质细胞,该脊髓已知参与行走,视觉或认知。它们比较了对应于不同残疾的区域之间的基因表达变化。在脊髓中 - 一个对行走至关重要的区域 - 它们发现胆固醇合成基因表达的降低。胆固醇不会离开血液并进入大脑,而是用星形胶质细胞制造,并在制作髓鞘,神经涂层和突触,神经连接中发挥作用。他们假设炎症导致骨髓苷和突触的损失,这是星形胶质细胞中胆固醇合成基因表达的降低,解释了为什么病变不在MS中修复。它们用胆固醇合成基因的表达增加的药物治疗小鼠 - 这导致了改善的行走能力。
影响
这种残疾的发现方法代表了寻找神经退行性疾病的神经保护治疗的策略,该疾病是针对每个残疾的修复损伤,与“一种尺寸适合所有”治疗方法相反。
作者
除了高级作者Rhonda Voskuhl博士外,他们指导了UCLA的多发性硬化方案,并在多发性硬化研究中持有杰克H. Skirball椅子,研究同事是Noriko Itoh,Yuichiro Itoh和Alessia Tassoni,与其他共同作者包括Emily Ren,Max Kaito,AI Ohno,Vista Farkhondeh,Hadley Johnsonbaugh,Yan Ao,Josh Burda和Michael Sofroniew,所有UCLA。
资金
该工作得到了康拉德N.希尔顿基金会的资金,国家卫生大学研究所,加州社区基金会,Tom Sharak MS Hope基金会,罗达Goetz基金会多发性硬化,以及UCLA多发性硬化症计划的其他合作伙伴。
出版物:Noriko Itoh,El Al。,“细胞特异性和区域特异性转录组织在多发性硬化模型中:专注于星形胶质细胞,“PNAS(2017)DOI:10.1073 / PNAS.1716032115
-
新技术照亮了AI系统的内部工作原理
2022-01-19 -
新的耶鲁学习揭示了ADHD作为不同疾病的集合
2022-01-19 -
UC研究人员揭示了大规模星系中的黑洞调节星形形成
2022-01-19 -
神经科学家发现控制时间的神经元网络
2022-01-18 -
科学家识别明确和隐含学习的神经签名
2022-01-18 -
研究表明硒保护了大脑中的内核
2022-01-16 -
星形丝状云的新模式
2022-01-14 -
星形丝状云的新模式
2022-01-14 -
哈佛学习对固定内存形成的主要模型进行了疑虑
2022-01-13 -
麻省理工学院的神经科学家确定了驱动愉悦行为的大脑回路
2022-01-12 -
“迷你大脑”揭示了失衡如何导致神经发育障碍
2022-01-11 -
“迷你大脑”揭示了失衡如何导致神经发育障碍
2022-01-11 -
“迷你大脑”揭示了失衡如何导致神经发育障碍
2022-01-11 -
“迷你大脑”揭示了失衡如何导致神经发育障碍
2022-01-11 -
本周的哈勃望远镜图像 - 螺旋星系NGC 4248
2022-01-09