可编程DNA技术“打印”细胞以创造多样的生物环境
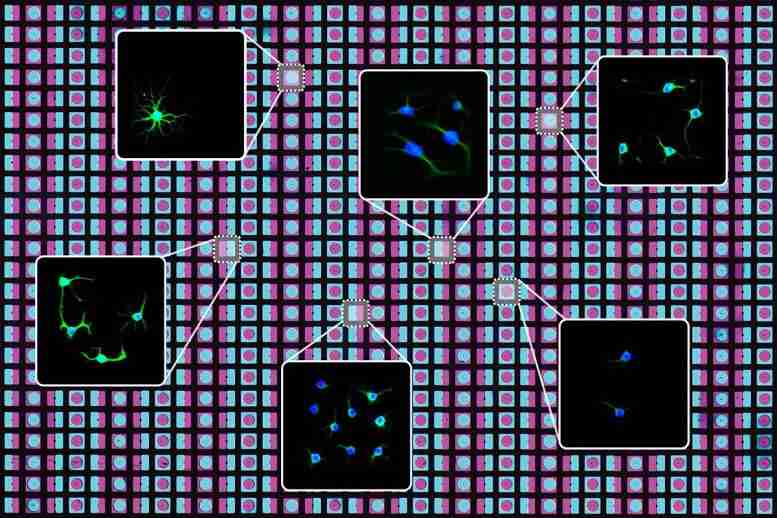
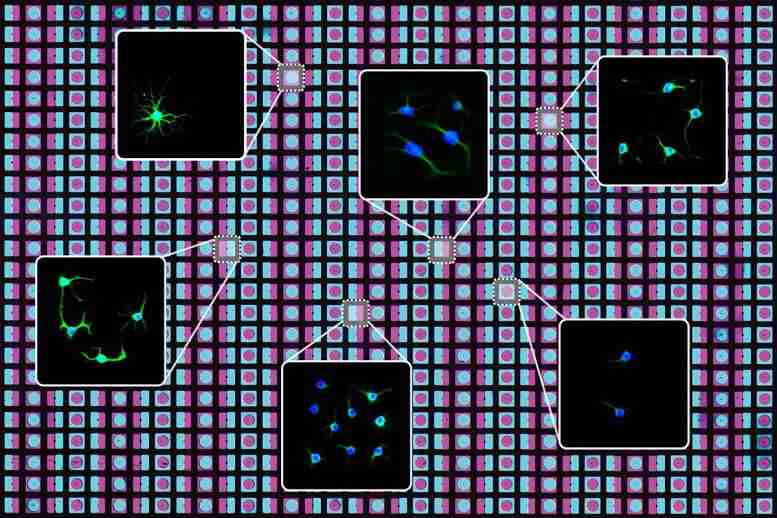
加利福尼亚大学伯克利分校的研究人员创造了一种新技术,该技术利用光刻技术和可编程DNA快速“打印”可模拟人体多种细胞环境的二维细胞和蛋白质阵列。
研究人员利用光刻技术和可编程DNA来快速构建模仿生活条件的细胞和蛋白质阵列。
像人类一样,细胞很容易受到同伴压力的影响。
以大脑中的神经干细胞为例:该细胞是保留的干细胞还是分化为完整的脑细胞,最终取决于细胞从无数个邻居那里收到的一系列复杂的分子信息。了解这些信息对于希望利用这些干细胞治疗神经系统疾病(如阿尔茨海默氏症或帕金森氏症)的科学家而言至关重要。
借助光刻技术和创造性DNA的创新使用,加州大学伯克利分校的研究人员创造了一种新技术,该技术可以快速“打印”细胞和蛋白质的二维阵列,以模拟体内多种细胞环境。 —是神经干细胞周围的大脑组织,肠或肝的内壁或肿瘤内部的细胞结构。
这项技术可以帮助科学家更好地理解决定细胞最终命运的复杂细胞间消息传递,从神经干细胞分化为脑细胞再到肿瘤细胞,并有可能转移到胚胎干细胞中。器官细胞。
“这个平台真正强大的功能是,您可以创建体外组织来捕获体内细胞的空间组织,从消化道的肠壁到肝脏中不同细胞类型的排列,” Olivia Scheideler说道。在伯克利读研究生时完成了研究。“我认为您可以将这种技术应用于想要探索细胞相互作用如何促进组织功能的任何组织。”
在今天(2020年3月18日星期三)在《科学进展》杂志上发表的一篇论文中,Scheideler及其合作者表明,这项新技术可用于将多达10种不同类型的细胞或蛋白质的复杂图案快速打印在平坦的表面上。
加州大学伯克利分校机械工程学教授,这篇论文的高级作者莱迪亚·索恩说:“本质上,这项技术使我们能够以一种高通量的方式一次成像各种条件。”“它非常灵活,为您学习的课程提供了广泛的选择范围。您可以对许多不同种类的细胞或蛋白质进行模式化。”
陷入DNA束缚
在新技术中,每个细胞或蛋白质都通过一串短链DNA束缚在基质上。尽管已经开发出类似的方法来将束缚的细胞或蛋白质一个接一个地附着,但这项新技术利用了称为光刻的构图过程,可以快速批量附着或打印每种类型的细胞蛋白质,从而大大加快了该过程。
“这就像彩色激光打印一样,先打印一种颜色,然后再打印另一种颜色,” Sohn说。
像摄影一样,光刻技术是通过将涂层表面或基材暴露在光的图案下而进行的,该光引发化学反应,该反应将涂层溶解在照明区域中,从而留下模板化的基材。在新技术中,然后将基板浸入单侧DNA链中,单侧DNA的末端已经过化学修饰,可以牢固地锁定在溶解涂层的位置。
每条单侧DNA链均经过编程,具有核苷酸腺嘌呤(A),胸腺嘧啶(T),鸟嘌呤(G)和胞嘧啶(C)的特定序列。具有互补核苷酸序列的单侧DNA链嵌入或附着在目标细胞或蛋白质上。
最后,用附着在单面DNA互补链上的细胞或蛋白质混合物洗涤表面,该混合物与已经附着在表面上的单面DNA结合形成双螺旋“系链”。
Sohn说:“由于DNA编程,所有的细胞和蛋白质都精确地附着在了它们应该存在的位置。”
通过重复此过程,最多可以将10种不同类型的细胞或蛋白质以任意模式拴在表面上。
冲突的消息
为了演示该技术的众多应用之一,Scheideler和合著者,加州大学伯克利分校的哈伯德·豪·哈伯德·豪·霍伊特生化工程杰出教授David Schaffer使用该平台研究了指示神经干细胞分化为成熟细胞的化学信号。 。
沙弗说:“干细胞的DNA内嵌有程序,可以告诉它们要么保留干细胞,要么分化成成熟细胞。”“他们从周围的环境以及周围的环境中获得了很多信息,该怎么办以及要从环境中激活哪些程序。如果我们能够学习如何使干细胞参与竞标,如何将它们转变成一种特定的细胞类型,那么我们就可以利用这些干细胞来大规模生产由于疾病或伤害而丢失的特殊细胞类型。”
舍德勒说,大脑中的神经干细胞会定期从邻居那里收到相互冲突的信息,说明它们的行为方式。一种信使,FGF-2蛋白,告诉他们制造更多的干细胞。另一个是ephrin-B2蛋白,告诉他们分化为成熟的神经元。
舍德勒使用这项新技术将神经干细胞图案化到两种蛋白质FGF-2和ephrin-B2的数千种不同阵列上,以了解这两种信号的空间组织如何帮助确定细胞的最终命运。
她发现,许多干细胞分化为成熟的神经元,即使它们主要与FGF-2接触,也就是“保持干细胞”使者。但是,当她近距离观察时,发现那些分化的细胞更可能具有细小的,手指状的延伸或“神经突”,触及了ephrin-B2或“分化”的信使。
“这种图案技术的伟大之处在于,您可以轻松地在幻灯片上复制这些小图案数百或数千次,” Schaffer说。就像进行一千个独立的小实验一样,每个实验都是一次试运行,以查看干细胞如何聆听其周围的细胞。然后,您可以获得有关其监管方式的非常非常深刻的统计数据。
参考:Olivia J. Scheideler,Chun Yang,Molly Kozminsky,Kira I. Mosher,RobertoFalcón-Banchs,Emma C. Ciminelli,Andrew W. Bremer,Sabrina A.撰写的“使用多重DNA构图方法概述复杂的生物信号环境”。 Chern,David V.Schaffer和Lydia L.Sohn,2020年3月18日,《科学进展》。
10.1126 / sciadv.aay5696
该论文的合著者包括加州大学伯克利分校的杨春,莫莉·科兹敏斯基,基拉·莫舍,罗伯托·法尔肯·班克斯,艾玛·C·西米内利和安德鲁·W·布雷默以及哈佛大学的萨布丽娜·A·切恩。
美国国立卫生研究院通过1R01CA190843-01、1R21EB019181-01A1,NIH / NCI F32 CA243354-01和1R21CA182375-01A1资助了这项研究。国家科学基金会研究生研究奖学金计划,Siebel Scholars计划和PEO奖学金也为该计划提供了支持。
-
蝎子毒液用于指导T细胞靶向脑癌肿瘤
2022-04-03 -
破解钩虫侵扰的代码 - 为疫苗提供新的希望
2022-04-03 -
孤独症和认知障碍之间的联系已确定–可能导致新的治疗方法
2022-04-03 -
蛋白质在没有治愈的儿童中罕见的疾病揭示的关键作用
2022-04-02 -
氟化物太多导致牙釉质缺陷 - 研究人员发现了原因
2022-04-01 -
麻省理工学院化学家调查疾病如何与缺陷的蛋白质折叠相关联
2022-04-01 -
生物学家被在不可预见的地方检测到的神经元的活动困扰
2022-03-31 -
通过激活免疫细胞来振兴衰老的大脑
2022-03-31 -
奇怪的海洋动物如何在其寿命中产生无限卵和精子的遗传秘诀
2022-03-31 -
新发明“凭空产生”电力–提供清洁能源24/7
2022-03-31 -
使用常用药物治愈脊柱损伤的新希望
2022-03-31 -
CRISPR-HOT:新的遗传工具可以标记特定的基因和细胞
2022-03-30 -
涉及味觉,阿尔茨海默氏症,哮喘的神秘细胞大洞的新发现
2022-03-30 -
新的单细胞产前DNA血液测试可以识别遗传异常
2022-03-29 -
新的蛋白质设计技术可以简化药物开发
2022-03-29