新的基因编辑技术可能被证明是一种有效的阻断HIV的技术
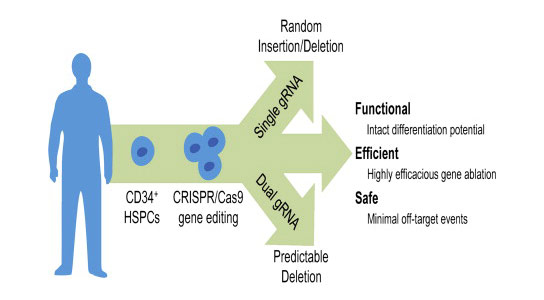
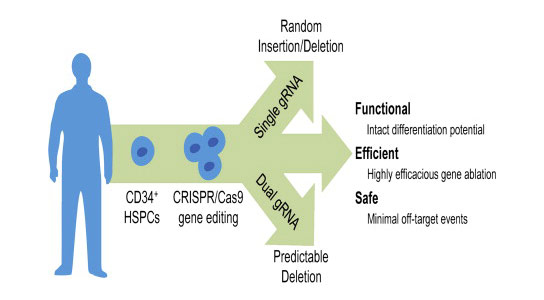
研究人员使用CRISPR Cas技术,通过基因“编辑”人类血液干细胞,创造出可能被证明是有效阻断HIV的技术。
麻省总医院(MGH)和波士顿儿童医院(BCH)的哈佛干细胞研究所(HSCI)的研究人员首次使用了一种相对较新的基因编辑技术来创建可以证明是一种有效的技术来阻止HIV的侵袭和入侵。破坏患者的免疫系统。
这是一组使用CRISPR Cas技术的首次发表的报告-它代表成簇的规则间隔的短回文重复激活细胞-可以有效,准确地从直接从人类收集的细胞中编辑出与临床相关的基因,在这种情况下,是人类造血干细胞和T细胞。
尽管研究人员认为,这种新的HIV治疗方法可能在不到五年的时间内就可以用于人体安全性试验,但他们自己提供了三个要点:首先也是最明显的是,它们可能会遇到意想不到的并发症。第二点是艾滋病毒/艾滋病的流行史上散布着“祸根”,事实证明并非如此。最后,即使这种新方法能完美发挥作用,它仍需要进行其他开发,以适用于该流行病最严重的地区。
这项研究由哈佛大学干细胞与再生生物学系副教授查德·科万(Chad Cowan)和德里克·罗西(Derrick Rossi)领导,并发表在《细胞干细胞》杂志上。
HIV专门针对构成血液免疫系统主要部分的T细胞,并通过称为CCR5的基因受体进入细胞,该基因作为进入细胞的门。一旦进入T细胞,HIV就会复制并杀死宿主细胞,使患者受各种机会感染的支配。
Cowan和Rossi团队使用CRISPR Cas基因编辑技术,从血干细胞中敲除了CCR5受体,他们发现这可能会导致没有CCR5的分化血细胞。从理论上讲,可以通过骨髓移植将这种经过基因编辑的干细胞引入HIV患者,该程序用于将血液干细胞移植到白血病患者中,从而产生抗HIV的免疫系统。
Cowan说:“我们证明了您可以非常有效地敲除CCR5,我们证明了细胞仍在起作用,并且我们进行了非常非常深入的测序分析以显示没有不需要的突变,因此看来是安全的。”他补充说:“显然还有很多工作要做。”
科恩说:“下一步是与马萨诸塞州拉贡研究所合作进行动物试验。”“有出色的小鼠模型,您可以赋予人类免疫系统,然后感染HIV。我们可以将细胞交给老鼠,看看它们是否受到艾滋病毒的保护。”一旦这些研究完成,并且如果成功并且没有出现并发症,下一步将是向美国食品药品监督管理局申请开展第一阶段人体试验,该试验仅用于测试新疗法的安全性。科恩说,现在尚无法预测这种审判将在多久之前开始。
血液学家/肿瘤学家戴维·斯卡登(David Scadden)既是HSCI的联合主任,又是MGH再生医学中心的主任,他称这项新工作“是编辑出使人类细胞容易感染HIV的巨大第一步。一个人自己的免疫细胞可以攻击艾滋病毒而又不易感染的想法成为可能。由于这是在干细胞中完成的,因此整个免疫系统可能会持久地感染病毒。这是一个强大的概念。
“这是我们从一路走到诊所必不可少的事情,”同时也是SCRB联合主席的Scadden说。他指出:“将需要进行相关研究以提高干细胞移植的安全性和便利性,才能将这项工作推广给广大患者,但是MGH慈善家的慷慨捐助带来了基因编辑和干细胞移植团队共同实现这一目标。”
使这项工作特别有前途的是,它可以为大批患者创造出一种方法,就像对“柏林患者”蒂莫西·雷·布朗所做的那样。柏林的医生给患有艾滋病毒/艾滋病和白血病的布朗提供了一种从患有罕见遗传缺陷的人身上获得的骨髓移植物,该人患有CCR5受体。据报道,自接受移植以来的六年中,布朗一直没有艾滋病毒感染,被认为是有史以来唯一“治愈”艾滋病毒/艾滋病的患者。如果成功的话,由Cowan和Rossi提出的基因疗法可能会完成同样的事情。
科恩说,该实验是HSCI进行的典型工作。干细胞生物学家小组刚刚“开始使用CRISPR系统,我正在与血液干细胞专家Derrick交谈,我们决定我们应该尝试一下。”因此,科恩(Cowan)和他的小组在T细胞中进行了基因编辑,而罗西(Rossi)的小组则专注于形成血液的干细胞。
Rossi说:“ CRISPR已经使用了将近两年,并且有报道指出在细胞系A或细胞系B中具有很高的功效。至今还没有人报道过CRISPR在原代血液干细胞中的功效或效用。”实验室位于波士顿儿童医院细胞与分子医学专业。“但是大多数研究人员同意,血液将成为基于基因编辑的疗法的首个目标组织。您可以从患者体内取出形成血液的干细胞,对其进行编辑,然后再移植回去。”
在他们的干细胞论文中,Rossi和Cowan表明他们可以高效β,可预测和精确地编辑T细胞中的2M和造血干/祖细胞(HSPC)中的CCR5。他们进一步表明,经过编辑的HSPC可以继续产生正常的血液和免疫细胞。
该对还解决了人们对CRISPR到底有多精确的担忧。
“有几篇论文表明,CRISPR具有很高的脱靶活性,” Rossi解释说。“我们决定在六种不同的实验条件下测试其在原代造血干细胞中的准确性。”
该团队对基因组中的位点进行了深度测序(与通常用于全基因组测序的50条相比,平均进行了3,400次测序),这可能会在尝试从HSPC中编辑CCR5时使CRISPR产生混淆。他们发现,该系统进行异常削减的风险实际上为零。同时,CCR5的预期靶向非常高。罗西说:“这些结果提供了临床前证据,即当将CRISPR 1.0版明智地用于造血干细胞中时,可很快为患者准备就绪。”
出版物:Pankaj K. Mandal等人,“使用CRISPR / Cas9有效消除人类造血干细胞和效应细胞中的基因”,《干细胞》,第15卷,第5期,第643-652页,2014年11月6日; doi:10.1016 / j.stem.2014.10.004
图像:Pankaj K.Mandal等。
-
新的基因编辑技术可能被证明是一种有效的阻断HIV的技术
2021-10-05 -
2型糖尿病和心血管疾病共有八种分子途径
2021-10-05 -
研究揭示了类似的“工具包”形状苍蝇,蠕虫和人类
2021-10-05 -
研究人员将人类多能干细胞重置为完全原始状态
2021-10-05 -
麻省理工学院工程师开发新技术以战斗超级培养
2021-10-05 -
新的声学装置将肿瘤细胞与血细胞分开
2021-10-05 -
听证会恢复噪音耳聋的老鼠
2021-10-04 -
新的生物技术创新降低了生物电路的不可预测性
2021-10-04 -
合成材料模拟生物体
2021-10-04 -
研究显示卡路里限制饮食缓慢老化
2021-10-04 -
UCLA科学家提出了一个更好的干细胞复制的基准
2021-10-04 -
以前未知的机制可在中风后修复大脑
2021-10-03 -
生物学家从实验室创造的细胞中生长起生物器官
2021-10-03 -
研究显示DNA变异形状的咖啡饮用习惯
2021-10-02 -
弱化癌症的新两步战略
2021-10-02